LH Family | 博骥源1类新药BGT-002在中国获批NASH适应症Ib/IIa临床研究
近日,博骥源(上海)生物医药有限公司新药管线核心品种BGT-002,ACLY(ATP依赖的柠檬酸裂解酶)小分子抑制剂,在中国获批非酒精性脂肪肝炎(NASH)新适应症的Ib/IIa临床研究,这也是国际上首个获批NASH适应症临床研究的ACLY小分子抑制剂。
》关于非酒精性脂肪肝(NAFLD及NASH)
非酒精性脂肪肝炎(NASH)是指在非酒精性脂肪肝病(NAFLD)的基础上具有更严重的肝小叶炎症和肝细胞损伤的病理状态。由于尚未有针对性药物上市,NASH成为肝硬化和肝癌的主要原因,严重影响着人类健康。据统计,NAFLD患病率25%,其中10-30%会发展成NASH。
随着生活水平的提高,NASH的发病正呈现全球高发态势,由2016年的3.1亿人上升到2020年的3.5亿人,复合年增长率为3.1%。预计全球NASH患者2025年达到4.1亿人,2030年将达4.8亿人,其中仅我国患者就将高达8000万。
NASH的发病进程中,脂质沉积是基础、炎症是核心、纤维化是病情恶化或者难以控制的关键因素。整体而言,数种因素造成的“多重打击”的复杂性导致其治疗药物研发难度巨大,以至于在过去的四十年间,绝大多数NASH药物研发均未取得突破性进展。国际上,除PPARα/γ双重激动剂Saroglitazar在印度获批上市用于治疗非肝硬化性NASH患者外,其它地区尚无一款NASH相关药物获批上市。近期,NASH新药研发已初现曙光。2022年12月19日,美国Madrigal公司研发的甲状腺激素受体β(THR-β)激动剂Resmetirom的III期临床研究达到主要终点和关键次要终点,该药很可能成为在世界主流市场获批上市的首款NASH治疗新药。
》关于ATP依赖的柠檬酸裂解酶(ACLY)
ATP依赖的柠檬酸裂解酶(ACLY)是一种以柠檬酸为底物的催化酶。ACLY将柠檬酸裂解生成为乙酰辅酶A,后者直接参与了脂质代谢、表观遗传调控等生命过程,因此ACLY抑制剂可通过多种途径发挥降血脂、降低心血管事件风险等作用。
不同于传统降血脂靶点,靶向抑制ACLY的活性对脂质合成与氧化、炎症细胞免疫调控、肝星状细胞活化调控等环节可发挥重要作用。近期的流行病学研究结果证实了ACLY的单核苷酸多态性(SNPs)与人类血清甘油三酯降低及NAFLD生物标志物之间存在紧密关联。作为一种代谢性疾病,非酒精性脂肪肝炎(NASH)的发病进程伴随了不同程度的肝脏脂质累积、炎症和纤维化等多种病理学危险信号的发生,其严重程度与可逆转性密切相关。因此,ACLY很可能成为下一个极具潜质的NAFLD及NASH新药研发靶标。
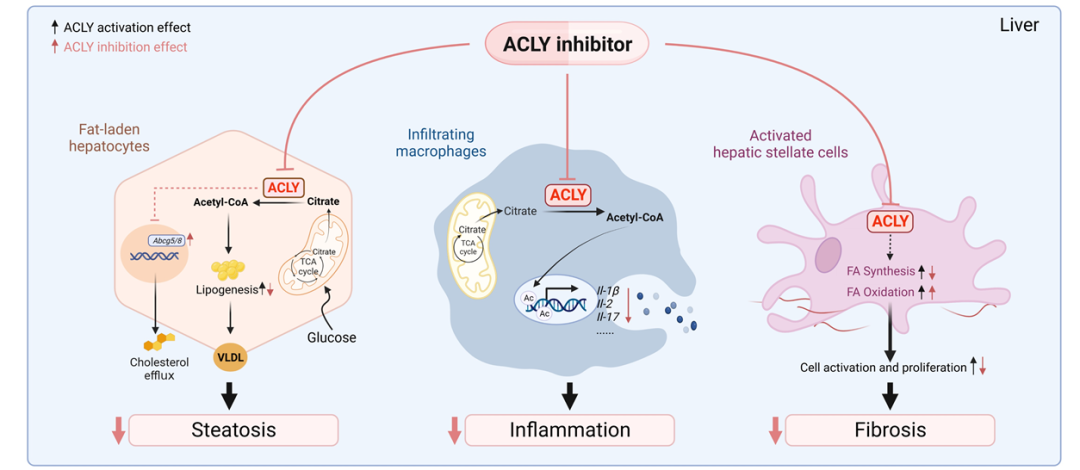
ACLY抑制剂通过多重机制显著改善NAFLD/NASH
》关于BGT-002
BGT-002是一种新型的靶向ACLY的小分子抑制剂,可有效改善高胆固醇血症。正在上海市徐汇区中心医院开展的Ⅰ期临床研究,已完成全部108名中国健康受试者的出组,初步人体用药安全性和有效性数据积极,药动学特征支持一天一次的口服给药方案,有望进一步开发后为众多他汀不耐受的高胆固醇患者提供新的用药选择。
此次BGT-002新获批适应症非酒精性脂肪肝(NAFLD及NASH),临床前研究显示,BGT-002在啮齿类和灵长类动物(老年食蟹猴)NASH药效模型中疗效显著。BGT-002是国际上首个获批该适应症并进入临床研究的ACLY小分子抑制剂,将按计划于2023年第一季度在NASH受试者上开展该项临床研究。
》关于博骥源
成立于2020年9月,博骥源以中国科学院上海药物研究所科学家团队对原始创新“病-靶-药”核心理念的高度认同为基础,深刻理解临床需求与病理机制(病)、严谨论证原创药物靶标(靶)、实践高效的临床前与临床研究开发(药),打造可持续发展的原始创新成果转化和产出平台,致力于真正中国原创的小分子新药研发。公司成立以来已陆续获得由领航新界、摩天石、昊苗健康领投的多轮融资。
自公司成立两年以来,已建立了丰富的创新药产品管线和候选新药储备。目前,公司抗血液恶性肿瘤1类新药BGT-001已完成Ⅰ期临床试验(单药),正开展三药全口服联用方案治疗复发难治性多发性骨髓瘤的多中心临床Ⅰb期研究;代谢性疾病1类新药BGT-002Ⅰ期临床研究已完成全部受试者出组,将于2023年第一季度在NASH受试者上开展临床Ⅰb/Ⅱa研究;炎症性肠病1类新药BGT-004已在2022年10月份递交pre-IND沟通,计划在2023年第一季度正式递交IND申报;公司另有多个代谢性疾病候选新药处于临床前开发阶段。
END



